Aminosäuren – Eigenschaften, Struktur, Klassifizierung und Funktionen

Aminosäuren sind die Bausteine von Proteinen und spielen eine Schlüsselrolle in zahlreichen biologischen Prozessen. Erfahren Sie alles über ihre physikalischen und chemischen Eigenschaften, ihre Klassifizierung und ihre Bedeutung für den menschlichen Organismus.
Was sind Aminosäuren?
Aminosäuren sind organische Verbindungen, die die funktionellen Eigenschaften von Aminen und Carbonsäuren kombinieren. Sie sind die grundlegenden Bausteine von Proteinen – Molekülen, die Gewebe, Organe und alle lebenswichtigen Systeme unseres Körpers aufbauen und erhalten. In der Natur wurden über 300 Arten von Aminosäuren entdeckt, aber nur 20 davon gelten als Standard, da sie direkt an der Proteinsynthese beteiligt sind und vom genetischen Code kodiert werden.
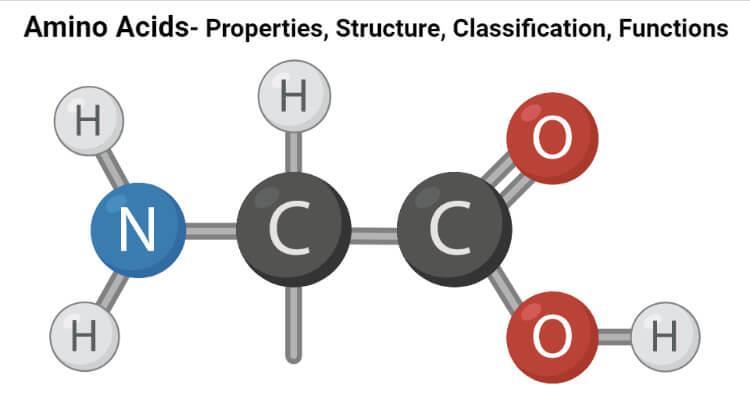
Jede Aminosäure besitzt eine gemeinsame Struktur – ein Alpha-Kohlenstoffatom, das mit einer Aminogruppe (–NH₂), einer Carboxylgruppe (–COOH), einem Wasserstoffatom und einer einzigartigen Seitenkette (R-Gruppe) verbunden ist, die die spezifischen Eigenschaften der jeweiligen Aminosäure bestimmt.
Physikalische Eigenschaften von Aminosäuren
Aminosäuren besitzen eine Reihe charakteristischer physikalischer Eigenschaften, die sie von anderen organischen Verbindungen unterscheiden:
- Kristalline Struktur: Alle Aminosäuren sind bei Raumtemperatur farblose kristalline Substanzen.
- Hoher Schmelzpunkt: Der Schmelzpunkt liegt bei den meisten Aminosäuren über 200°C.
- Löslichkeit: Sie sind gut in Wasser löslich, in Alkoholen (Methanol, Ethanol, Propanol) schlechter. Die Löslichkeit hängt von der Art der R-Gruppe und dem pH-Wert der Umgebung ab.
- Thermische Instabilität: Beim Erhitzen auf hohe Temperaturen zersetzen sich Aminosäuren.
- Optische Aktivität: Alle Aminosäuren außer Glycin sind optisch aktiv – sie können die Ebene des polarisierten Lichts drehen.
- Peptidbindung: Aminosäuren können sich über eine kovalente Peptidbindung (–CO–NH–) verbinden, die zwischen der Aminogruppe der einen und der Carboxylgruppe der anderen Aminosäure gebildet wird.
Chemische Eigenschaften
Zwitterionische Natur
Ein Zwitterion ist ein Molekül, das gleichzeitig eine positive und eine negative Ladung trägt, wobei die gesamte Nettoladung Null ist. In Lösung liegen Aminosäuren überwiegend in dieser Form vor – die Aminogruppe nimmt ein Proton (H⁺) von der Carboxylgruppe auf, wodurch eine innere Salzstruktur entsteht. Dies ist auch die Hauptform, in der Aminosäuren in biologischen Flüssigkeiten vorkommen.
Amphotere Eigenschaften
Aufgrund der Anwesenheit sowohl einer Amino- als auch einer Carboxylgruppe zeigen Aminosäuren amphotere Eigenschaften – sie können je nach pH-Wert der Umgebung sowohl als Säuren als auch als Basen wirken.
Ninhydrin-Reaktion
Eine der verbreitetsten qualitativen Reaktionen: Bei Zugabe einer Ninhydrin-Lösung zu einer Aminosäure und Erhitzen bildet sich eine charakteristische violette Färbung, die das Vorhandensein von α-Aminosäuren bestätigt.
Xanthoprotein-Reaktion
Diese Reaktion wird zum Nachweis von aromatischen Aminosäuren (Tyrosin, Tryptophan und Phenylalanin) verwendet. Bei Behandlung mit Salpetersäure wird eine charakteristische gelbe Färbung beobachtet, die auf die Nitrierung der aromatischen Ringe in den Seitenketten zurückzuführen ist.
Reaktion mit Sanger-Reagenz
Das Sanger-Reagenz (1-Fluor-2,4-dinitrobenzol) reagiert in schwach alkalischer Umgebung mit der Aminogruppe der Peptidkette, was die Bestimmung der N-terminalen Aminosäure in der Proteinfolge ermöglicht.
Reaktion mit salpetriger Säure
Bei der Reaktion mit salpetriger Säure wird die Aminogruppe unter Abspaltung von molekularem Stickstoff (N₂) eliminiert, und an ihrer Stelle bildet sich eine Hydroxylgruppe.
Struktur von Aminosäuren
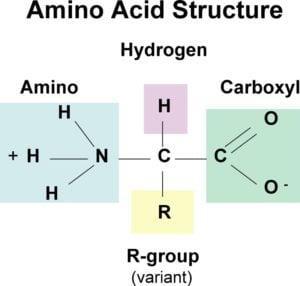
Alle 20 Standard-Aminosäuren sind α-Aminosäuren – sie enthalten eine Carboxylgruppe, eine Aminogruppe und eine Seitenkette (R-Gruppe), die an dasselbe α-Kohlenstoffatom gebunden sind. Die Grundkette ist für alle Aminosäuren identisch, die Einzigartigkeit wird durch die R-Gruppe bestimmt.
Bemerkenswerte Ausnahmen:
- Glycin – die einfachste Aminosäure, ohne Seitenkette (R = H). Sie ist optisch nicht aktiv, da ihr ein asymmetrisches Kohlenstoffatom fehlt.
- Prolin – die einzige Standard-Aminosäure, bei der das Stickstoffatom Teil einer zyklischen Struktur (Pyrrolidinring) ist.
Alle anderen 19 Aminosäuren haben die L-Konfiguration um das α-Kohlenstoffatom – dies ist die natürliche stereochemische Form, die von lebenden Organismen verwendet wird.
Klassifizierung von Aminosäuren
Klassifizierung nach Art der Seitenkette (R-Gruppe)
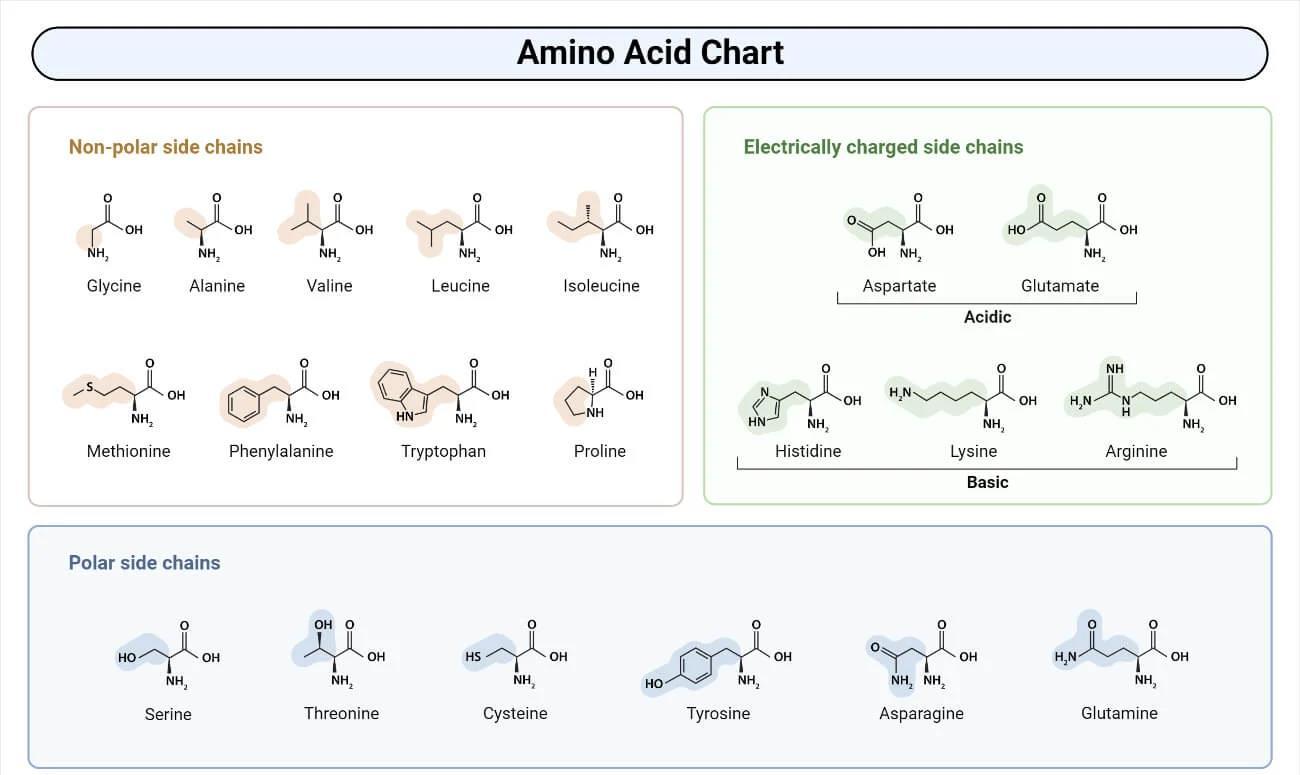
- Unpolare aliphatische Aminosäuren: Haben hydrophobe Seitenketten – Glycin, Alanin, Valin, Leucin, Isoleucin, Methionin und Prolin.
- Aromatische Aminosäuren: Phenylalanin, Tyrosin und Tryptophan – mit aromatischen Ringen in der R-Gruppe, die an hydrophoben Wechselwirkungen beteiligt sind.
- Polare ungeladene Aminosäuren: Serin, Threonin, Cystein, Asparagin und Glutamin – mit hydrophilen R-Gruppen, die Wasserstoffbrückenbindungen bilden.
- Saure (negativ geladene) Aminosäuren: Glutaminsäure und Asparaginsäure.
- Basische (positiv geladene) Aminosäuren: Lysin, Arginin und Histidin.
Klassifizierung nach ernährungsphysiologischer Unentbehrlichkeit
| Unentbehrlich (essentiell) | Bedingt unentbehrlich | Entbehrlich |
|---|---|---|
| Histidin | Arginin | Alanin |
| Isoleucin | Cystin | Asparagin |
| Leucin | Glutamin | Aspartat |
| Lysin | Glycin | Glutamat |
| Methionin | Prolin | Serin |
| Phenylalanin | Tyrosin | |
| Threonin | ||
| Tryptophan | ||
| Valin |
Unentbehrliche Aminosäuren (9 Stück): Der Körper kann sie nicht selbst synthetisieren, daher müssen sie über die Nahrung aufgenommen werden – Histidin, Isoleucin, Leucin, Lysin, Methionin, Phenylalanin, Threonin, Tryptophan und Valin.
Entbehrliche und bedingt entbehrliche Aminosäuren (11 Stück): Können im Körper synthetisiert werden, aber unter bestimmten Bedingungen (Stress, intensive Trainingseinheiten, Krankheit) kann der Bedarf die Produktionskapazität übersteigen.
Klassifizierung nach metabolischer Bestimmung
| Glukogen | Glukogen und ketogen | Ketogen |
|---|---|---|
| Alanin, Arginin, Asparagin, Aspartat, Cystein, Glutamat, Glutamin, Glycin, Histidin, Methionin, Prolin, Serin, Threonin, Valin | Isoleucin, Phenylalanin, Tryptophan, Tyrosin | Leucin, Lysin |
- Glukogen: Dienen als Vorläufer für die Glukosebildung durch Glukoneogenese.
- Ketogen: Bilden bei ihrem Abbau Ketonkörper (Leucin und Lysin).
- Gemischt: Können sowohl Glukose als auch Ketonkörper bilden.
Funktionen von Aminosäuren im Körper
Aminosäuren erfüllen äußerst vielfältige Funktionen, ohne die eine normale Körperfunktion unmöglich ist:
- Bausteinfunktion: Die zwanzig Standard-Aminosäuren sind die grundlegenden „Bausteine", aus denen alle Proteine und Peptide in lebenden Organismen aufgebaut werden.
- Strukturinformation: Die lineare Abfolge der Aminosäuren in der Polypeptidkette bestimmt die dreidimensionale Konfiguration des Proteins, und von der Struktur hängt seine Funktion ab.
- Hormonsynthese: Beteiligt an der Produktion von Hormonen (Adrenalin, Schilddrüsenhormone, Insulin).
- Muskelstruktur: Ermöglicht den Aufbau und die Reparatur von Muskelgewebe – von entscheidender Bedeutung für Sportler und intensiv Trainierende.
- Nervensystem: Dienen als Vorläufer für Neurotransmitter (Serotonin, Dopamin, GABA) und erhalten die gesunde Funktion des Zentralnervensystems aufrecht.
- Energiestoffwechsel: Bei Bedarf werden Aminosäuren zur Energiegewinnung oxidiert, insbesondere bei längeren körperlichen Belastungen.
- Biosynthese: Beteiligt an der Synthese von Purinen, Pyrimidinen, Porphyrinen, Kreatin und anderen lebenswichtigen stickstoffhaltigen Verbindungen.
💡 Expertenurteil
Um den Bedarf an allen unentbehrlichen Aminosäuren optimal zu decken, kombinieren Sie verschiedene Proteinquellen – Molkenprotein, Eier, Hülsenfrüchte und Getreide. Bei intensivem Training kann die Ergänzung mit BCAAs (Leucin, Isoleucin, Valin) die Muskelregeneration unterstützen und den Katabolismus reduzieren.
🧭 Wann wählen Sie was?
- Wählen Sie einzelne Aminosäuren, wenn Sie eine schnelle Aufnahme für einen bestimmten Zweck (z. B. nach dem Training) anstreben oder einen spezifischen Mangel haben.
- Wählen Sie Proteinpräparate (mit verschiedenen Aminosäuren), wenn Sie umfassende Unterstützung für Muskelwachstum und allgemeine Erholung suchen.
- Priorisieren Sie vollwertige Protein-Nahrungsquellen, wenn Sie langfristige Gesundheit, ausgewogene Ernährung und die Zufuhr aller essentiellen Nährstoffe anstreben.
📖 Was sind Aminosäuren?
Aminosäuren sind die Bausteine von Proteinen. Sie verbinden sich miteinander, um lange Ketten zu bilden, die Muskeln, Enzyme und andere wichtige Körperstrukturen aufbauen. Es gibt 20 Hauptaminosäuren, von denen 9 essentiell sind, was bedeutet, dass der Körper sie nicht selbst herstellen kann.
⚖️ Vorteile und Nachteile
| ✅ Vorteile | ❌ Nachteile |
|---|---|
|
|
🗣️ Einfach erklärt
Aminosäuren sind die grundlegenden Bausteine von Proteinen, wie Ziegelsteine, aus denen deine Muskeln gebaut werden. Es gibt verschiedene Arten, manche macht dein Körper selbst, andere musst du über die Nahrung aufnehmen. Sie sind super wichtig für Muskeln, Haut, Haare und fast alles in deinem Körper.