Aminoacizi – proprietăți, structură, clasificare și funcții

Aminoacizii sunt elementele constitutive ale proteinelor și joacă un rol cheie într-o multitudine de procese biologice. Aflați totul despre proprietățile lor fizice și chimice, clasificarea și importanța lor pentru organismul uman.
Ce sunt aminoacizii?
Aminoacizii sunt compuși organici care combină proprietățile funcționale ale aminelor și ale acizilor carboxilici. Aceștia sunt blocurile de bază ale proteinelor — moleculele care construiesc și susțin țesuturile, organele și toate sistemele vitale din corpul nostru. Peste 300 de tipuri de aminoacizi au fost descoperite în natură, dar doar 20 dintre ei sunt considerați standard, deoarece participă direct la sinteza proteinelor și sunt codificați de codul genetic.
Fiecare aminoacid are o bază structurală comună — un atom de carbon alfa, legat de o grupare amino (–NH₂), o grupare carboxil (–COOH), un atom de hidrogen și o catenă laterală unică (grupare R), care determină proprietățile specifice ale aminoacidului respectiv.
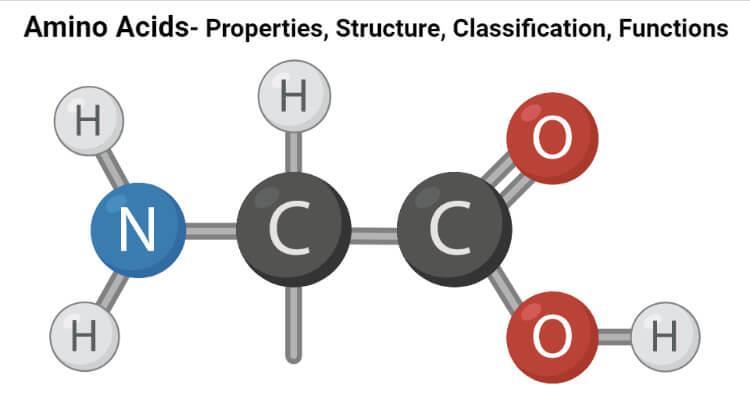
Proprietăți fizice ale aminoacizilor
Aminoacizii au o serie de proprietăți fizice caracteristice care îi diferențiază de alte compuși organici:
- Structură cristalină: Toți aminoacizii sunt substanțe cristaline incolore la temperatura camerei.
- Punct de topire ridicat: Punctul de topire depășește 200°C pentru majoritatea aminoacizilor.
- Solubilitate: Sunt bine solubili în apă, mai puțin — în alcooli (metanol, etanol, propanol). Solubilitatea depinde de caracterul grupării R și de pH-ul mediului.
- Instabilitate termică: La încălzirea la temperaturi înalte, aminoacizii se descompun.
- Activitate optică: Toți aminoacizii, cu excepția glicinei, sunt optici activi — capabili să rotească planul luminii polarizate.
- Legătură peptidică: Aminoacizii se pot lega între ei printr-o legătură peptidică covalentă (–CO–NH–), formată între gruparea amino a unuia și gruparea carboxil a altui aminoacid.
Proprietăți chimice
Natură zwitterionică
Zwitterionul este o moleculă care poartă simultan o sarcină pozitivă și una negativă, sarcina netă totală fiind zero. În soluție, aminoacizii există predominant sub această formă — gruparea amino acceptă un proton (H⁺) de la gruparea carboxil, formând o structură de sare internă. Aceasta este și forma principală în care aminoacizii sunt prezenți în lichidele biologice.
Proprietăți amfoterice
Datorită prezenței atât a grupării amino, cât și a celei carboxil, aminoacizii manifestă o natură amfoteră — pot acționa atât ca acizi, cât și ca baze, în funcție de pH-ul mediului.
Reacția cu ninhidrina
Una dintre cele mai răspândite reacții calitative: la adăugarea unei soluții de ninhidrină la un aminoacid și încălzire, se formează o colorație violetă caracteristică, care confirmă prezența α-aminoacizilor.
Reacția xantoproteică
Această reacție este utilizată pentru detectarea aminoacizilor aromatici (tirozină, triptofan și fenilalanină). La tratarea cu acid azotic, se observă o colorație galbenă caracteristică, datorată nitrării inelelor aromatice din lanțurile laterale.
Reacția cu reactivul Sanger
Reactivul Sanger (1-fluoro-2,4-dinitrobenzen) reacționează cu gruparea amino a lanțului peptidic într-un mediu slab alcalin, permițând determinarea aminoacidului N-terminal din secvența proteică.
Reacția cu acidul azotos
În interacțiunea cu acidul azotos, gruparea amino este eliminată cu eliberarea de azot molecular (N₂), iar în locul ei se formează o grupare hidroxil.
Structura aminoacizilor
Toți cei 20 de aminoacizi standard sunt α-aminoacizi — conțin o grupare carboxil, o grupare amino și o catenă laterală (grupare R), legate de același atom de carbon α. Lanțul de bază este identic pentru toți aminoacizii, iar unicitatea este determinată de gruparea R.
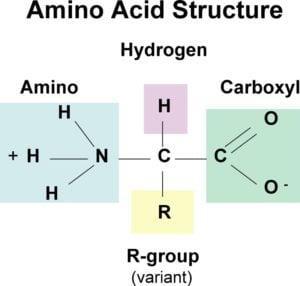
Excepții notabile:
- Glicină — cel mai simplu aminoacid, fără catenă laterală (R = H). Nu este optic activă din cauza lipsei unui carbon asimetric.
- Prolină — singurul aminoacid standard la care atomul de azot face parte dintr-o structură ciclică (inel pirolidinic).
Toți ceilalți 19 aminoacizi au configurație L în jurul carbonului α — aceasta este forma stereochimică naturală utilizată de organismele vii.
Clasificarea aminoacizilor
Clasificare după caracterul catenei laterale (gruparea R)
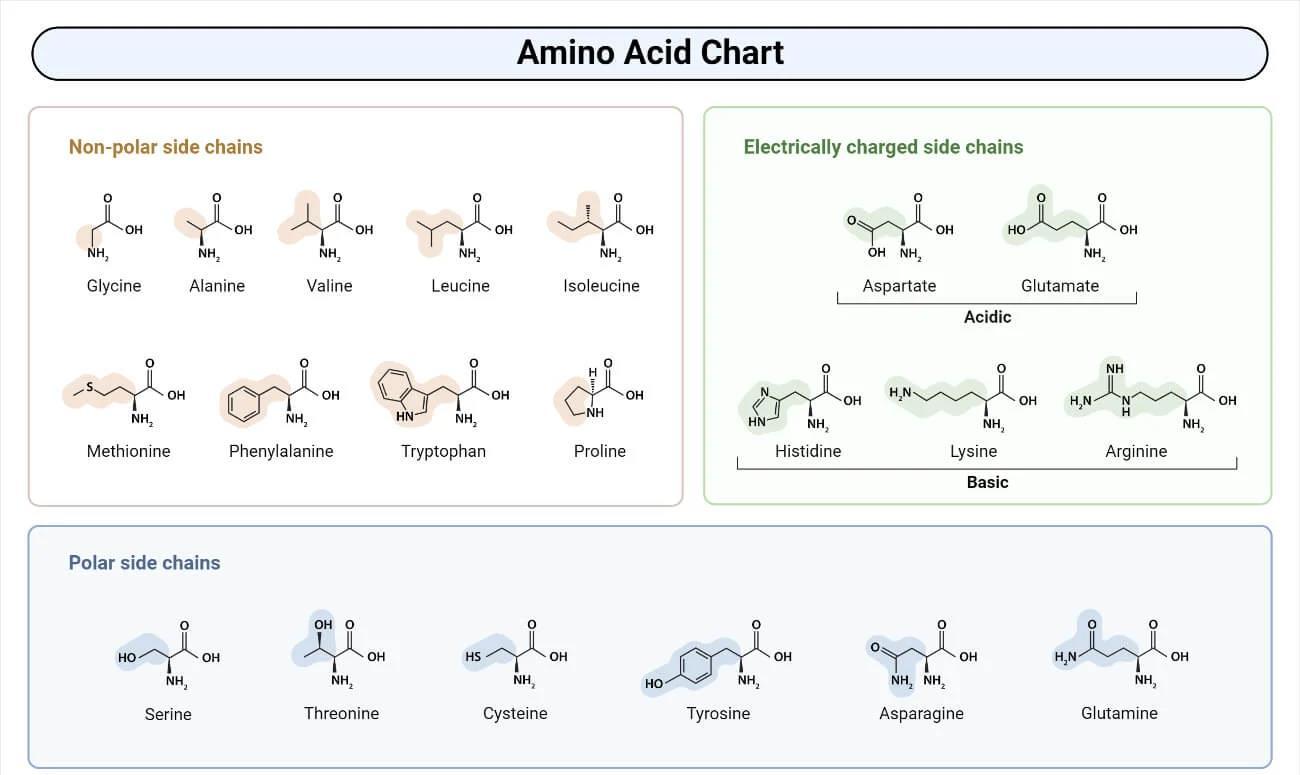
- Aminoacizi alifatici nepolari: Au lanțuri laterale hidrofobe — glicină, alanină, valină, leucină, izoleucină, metionină și prolină.
- Aminoacizi aromatici: Fenilalanină, tirozină și triptofan — cu inele aromatice în gruparea R, implicate în interacțiuni hidrofobe.
- Aminoacizi polari neîncărcați: Serină, treonină, cisteină, asparagină și glutamină — cu grupări R hidrofile, care formează legături de hidrogen.
- Aminoacizi acizi (încărcați negativ): Acid glutamic și acid aspartic.
- Aminoacizi bazici (încărcați pozitiv): Lizină, arginină și histidină.
Clasificare după indispensabilitatea alimentară
| Indispensabili (esențiali) | Condiționat indispensabili | Detașabili |
|---|---|---|
| Histidină | Arginină | Alanină |
| Izoleucină | Cisteină | Asparagină |
| Leucină | Glutamină | Aspartat |
| Lizina | Glicină | Glutamat |
| Metionină | Prolină | Serină |
| Fenilalanină | Tirozină | |
| Treonină | ||
| Triptofan | ||
| Valină |
Aminoacizi indispensabili (9 la număr): Organismul nu îi poate sintetiza singur, de aceea trebuie furnizați prin alimentație — histidină, izoleucină, leucină, lizină, metionină, fenilalanină, treonină, triptofan și valină.
Aminoacizi detașabili și condiționat detașabili (11 la număr): Pot fi sintetizați în organism, dar în anumite condiții (stres, antrenamente intense, boală) nevoia de aceștia poate depăși capacitatea de producție.
Clasificare după destinul metabolic
| Glicogenici | Glicogenici și cetogenici | Cetogenici |
|---|---|---|
| Alanină, Arginină, Asparagină, Aspartat, Cisteină, Glutamat, Glutamină, Glicină, Histidină, Metionină, Prolină, Serină, Treonină, Valină | Izoleucină, Fenilalanină, Triptofan, Tirozină | Leucină, Lizină |
- Glicogenici: Servesc ca precursori pentru formarea glucozei prin gluconeogeneză.
- Cetogenici: La descompunere formează corpuri cetonice (leucină și lizină).
- Mixti: Pot da naștere atât glucozei, cât și corpilor cetonici.
Funcțiile aminoacizilor în organism
Aminoacizii îndeplinesc funcții extrem de diverse, fără de care funcționarea normală a organismului este imposibilă:
- Funcție de construcție: Cei douăzeci de aminoacizi standard sunt „cărămizile" de bază din care sunt construite toate proteinele și peptidele din organismele vii.
- Informație structurală: Secvența liniară a aminoacizilor dintr-un lanț polipeptidic determină configurația tridimensională a proteinei, iar de structură depinde funcția acesteia.
- Sinteza hormonilor: Participă la producerea hormonilor (adrenalină, hormoni tiroidieni, insulină).
- Structura musculară: Asigură construirea și refacerea țesuturilor musculare — de o importanță excepțională pentru sportivi și cei care se antrenează activ.
- Sistem nervos: Servesc ca precursori ai neurotransmițătorilor (serotonină, dopamină, GABA) și susțin funcționarea sănătoasă a sistemului nervos central.
- Metabolism energetic: La nevoie, aminoacizii sunt oxidați pentru a obține energie, în special în timpul eforturilor fizice prelungite.
- Biosinteză: Participă la sinteza purinelor, pirimidinelor, porfirinelor, creatinei și altor compuși azotati vitali.
💡 Concluzie expert
Pentru a acoperi optim necesarul tuturor aminoacizilor indispensabili, combinați surse proteice variate — proteină din zer, ouă, leguminoase și cereale. În timpul antrenamentelor intense, suplimentarea cu BCAA (leucină, izoleucină, valină) poate sprijini recuperarea musculară și reduce catabolismul.
🧭 Când să alegeți ce?
- Alegeți aminoacizi individuali dacă vizați o absorbție rapidă pentru un scop specific (de ex. recuperare post-antrenament) sau aveți un deficit specific.
- Alegeți suplimente proteice (conținând diverse aminoacizi) dacă căutați suport complex pentru creșterea musculară și recuperare generală.
- Prioritizați sursele de proteine integrale din alimentație dacă vizați sănătatea pe termen lung, o nutriție echilibrată și aportul tuturor nutrienților esențiali.
📖 Ce sunt Aminoacizii?
Aminoacizii sunt elementele constitutive ale proteinelor. Se leagă între ei pentru a forma lanțuri lungi care construiesc mușchii, enzimele și alte structuri importante ale corpului. Există 20 de aminoacizi principali, dintre care 9 sunt esențiali, ceea ce înseamnă că organismul nu îi poate produce singur.
⚖️ Avantaje și Dezavantaje
| ✅ Avantaje | ❌ Dezavantaje |
|---|---|
|
|
🗣️ Explicat simplu
Aminoacizii sunt elementele de bază ale proteinelor, ca niște cărămizi din care îți sunt construiți mușchii. Există diferite tipuri, unii pe care corpul tău îi produce singur, alții pe care trebuie să-i obții din alimentație. Sunt super importanți pentru mușchi, piele, păr și aproape totul în corpul tău.