Аминокиселине – својства, структура, класификација и функције

Аминокиселините су градивни елементи протеина и играју кључну улогу у бројним биолошким процесима. Сазнајте све о њиховим физичким и хемијским својствима, класификацији и значају за људски организам.
Шта су аминокиселине?
Аминокиселине су органска једињења која комбинују функционална својства амина и карбоксилних киселина. Оне су основни градивни блокови протеина — молекула које изграђују и одржавају ткива, органе и све виталне системе у нашем телу. У природи је откривено преко 300 врста аминокиселина, али само 20 њих се сматра стандардним, јер директно учествују у синтези протеина и кодиране су генетским кодом.
Свака аминокиселина има заједничку структурну основу — алфа-угљеников атом повезан са аминогрупом (–NH₂), карбоксилном групом (–COOH), атомом водоника и јединственим бочним ланцем (R-група), који одређује специфична својства одговарајуће аминокиселине.
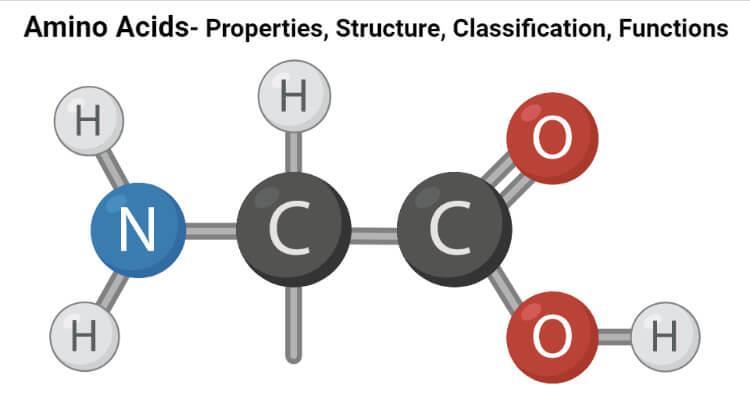
Физичка својства аминокиселина
Аминокиселине поседују низ карактеристичних физичких својстава која их разликују од осталих органских једињења:
- Кристална структура: Све аминокиселине су безбојне кристални супстанце на собној температури.
- Висока тачка топљења: Тачка топљења прелази 200°C за већину аминокиселина.
- Растворљивост: Добро су растворљиве у води, мање — у алкохолима (метанол, етанол, пропанол). Растворљивост зависи од карактера R-групе и pH средине.
- Термичка нестабилност: При загревању на високе температуре аминокиселине се разлажу.
- Оптичка активност: Све аминокиселине, осим глицина, су оптички активне — способне да ротирају раван поларизоване светлости.
- Пептидна веза: Аминокиселине се могу повезивати једна са другом ковалентном пептидном везом (–CO–NH–), формираном између аминогрупе једне и карбоксилне групе друге аминокиселине.
Хемијска својства
Цвитерионска природа
Цвитерион је молекула која носи истовремено позитиван и негативан набој, при чему је укупан нето набој нула. У раствору, аминокиселине углавном постоје у овом облику — аминогрупа прима протон (H⁺) из карбоксилне групе, формирајући унутрашњу солну структуру. Ово је и основни облик у којем се аминокиселине налазе у биолошким течностима.
Амфотерна својства
Захваљујући присуству и амино- и карбоксилне групе, аминокиселине показују амфотерну природу — могу деловати и као киселине и као базе, у зависности од pH средине.
Нихидринска реакција
Једна од најраспрострањенијих квалитативних реакција: при додавању нихидринског раствора аминокиселини и загревању, формира се карактеристично љубичасто обојење, које потврђује присуство α-аминокиселина.
Ксантопротеинска реакција
Ова реакција се користи за откривање ароматичних аминокиселина (тирозин, триптофан и фенилаланин). При третирању азотном киселином, примећује се карактеристично жуто обојење, које је последица нитрирања ароматичних прстенова у бочним ланцима.
Реакција са Сангеровим реагенсом
Сангеров реагент (1-флуоро-2,4-динитробензен) реагује са аминогрупом пептидног ланца у слабо алкалној средини, што омогућава одређивање N-терминалне аминокиселине у протеинском низу.
Реакција са азотном киселином
При интеракцији са азотном киселином, аминогрупа се елиминише уз ослобађање молекуларног азота (N₂), а на њеном месту се формира хидроксилна група.
Структура аминокиселина
Свих 20 стандардних аминокиселина су α-аминокиселине — садрже карбоксилну групу, аминогрупу и бочни ланац (R-групу), повезане са истим α-угљениковим атомом. Основни ланац је идентичан за све аминокиселине, а јединственост се одређује R-групом.
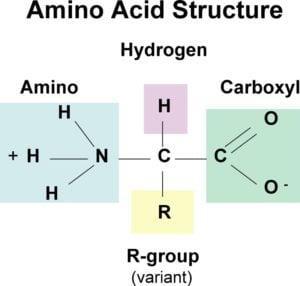
Значајни изузеци:
- Глицин — најједноставнија аминокиселина, без бочног ланца (R = H). Није оптички активан због недостатка асиметричног угљеника.
- Пролин — једина стандардна аминокиселина код које је атом азота део цикличне структуре (пиролидински прстен).
Свих осталих 19 аминокиселина имају L-конфигурацију око α-угљеника — ово је природни стереохемијски облик који користе живи организми.
Класификација аминокиселина
Класификација по карактеру бочног ланца (R-група)
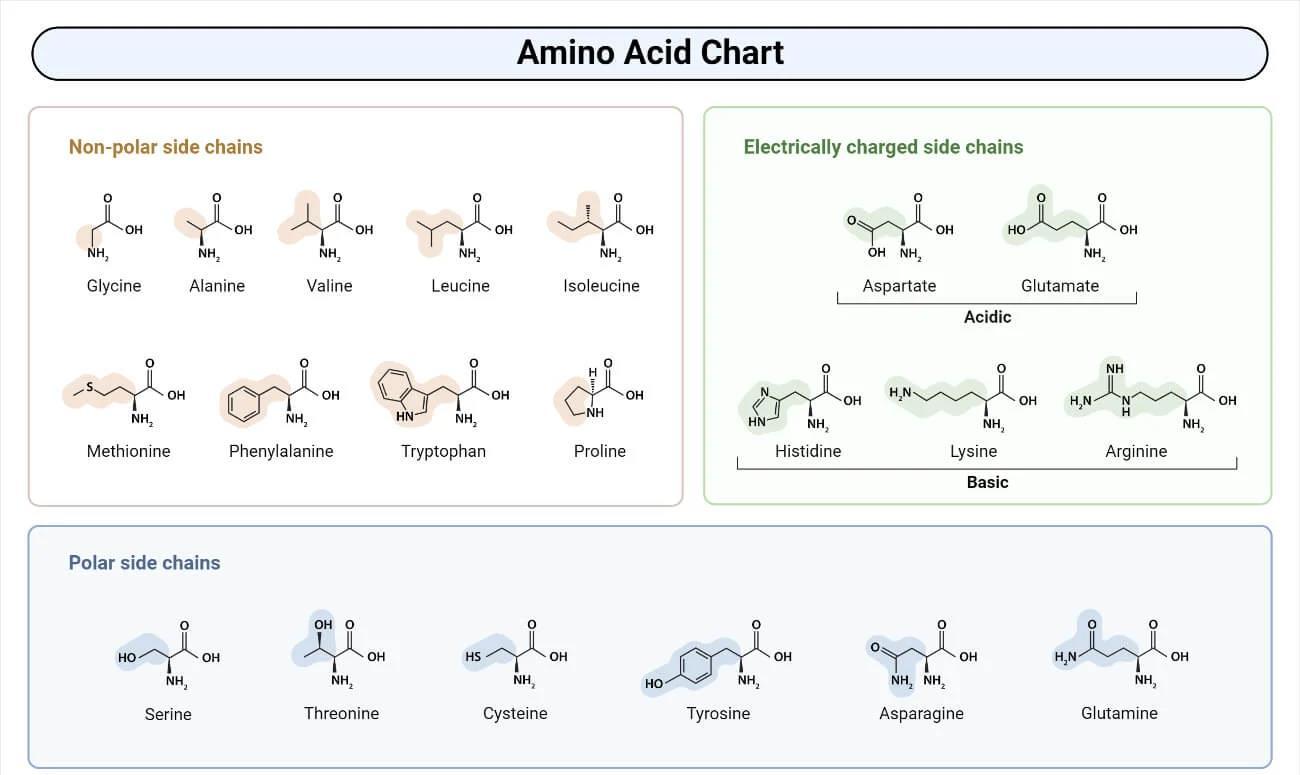
- Неполарне алифатичне аминокиселине: Имају хидрофобне бочне ланце — глицин, аланин, валин, леуцин, изолеуцин, метионин и пролин.
- Ароматичне аминокиселине: Фенилаланин, тирозин и триптофан — са ароматичним прстеновима у R-групи, који учествују у хидрофобним интеракцијама.
- Поларне незаређене аминокиселине: Серин, треонин, цистеин, аспарагин и глутамин — са хидрофилним R-групама, које формирају водоничне везе.
- Киселе (негативно наелектрисане) аминокиселине: Глутаминска и аспаргинска киселина.
- Базне (позитивно наелектрисане) аминокиселине: Лизин, аргинин и хистидин.
Класификација по нутритивној неопходности
| Неопходне (есенцијалне) | Условно неопходне | Заменљиве |
|---|---|---|
| Хистидин | Аргинин | Аланин |
| Изолеуцин | Цистин | Аспарагин |
| Леуцин | Глутамин | Аспартат |
| Лизин | Глицин | Глутамат |
| Метионин | Пролин | Серин |
| Фенилаланин | Тирозин | |
| Треонин | ||
| Триптофан | ||
| Валин |
Неопходне аминокиселине (9 бројева): Организам их не може сам синтетизовати, стога се морају уносити путем исхране — хистидин, изолеуцин, леуцин, лизин, метионин, фенилаланин, треонин, триптофан и валин.
Заменљиве и условно заменљиве аминокиселине (11 бројева): Могу се синтетизовати у организму, али под одређеним условима (стрес, интензивни тренинзи, болест) потреба за њима може надмашити производни капацитет.
Класификација по метаболичкој судбини
| Гликогене | Гликогене и кетогене | Кетогене |
|---|---|---|
| Аланин, Аргинин, Аспарагин, Аспартат, Цистеин, Глутамат, Глутамин, Глицин, Хистидин, Метионин, Пролин, Серин, Треонин, Валин | Изолеуцин, Фенилаланин, Триптофан, Тирозин | Леуцин, Лизин |
- Гликогене: Служе као прекурсори за стварање глукозе путем глуконеогенезе.
- Кетогене: При разградњи образују кетонска тела (леуцин и лизин).
- Мешовите: Могу дати почетак како глукози, тако и кетонским телима.
Функције аминокиселина у организму
Аминокиселине обављају изузетно разноврсне функције, без којих је нормално функционисање организма немогуће:
- Градивна функција: Двадесет стандардних аминокиселина су основни „цигле" од којих се граде сви протеини и пептиди у живим организмима.
- Структурне информације: Линеарни низ аминокиселина у полипептидном ланцу одређује тродимензионалну конфигурацију протеина, а од структуре зависи његова функција.
- Хормонски синтез: Учествују у производњи хормона (адреналин, тироидни хормони, инсулин).
- Мишићна структура: Обезбеђују изградњу и опоравак мишићних ткива — од изузетног значаја за спортисте и активно тренирајуће.
- Нервни систем: Служе као прекурсори неуротрансмитера (серотонин, допамин, ГАМК) и одржавају здраво функционисање централног нервног система.
- Енергетски метаболизам: Ако је потребно, аминокиселине се оксидују ради добијања енергије, посебно при продуженим физичким оптерећењима.
- Биосинтеза: Учествују у синтези пурина, пиримидина, порфирина, креатина и других виталних азотних једињења.
💡 Експертски закључак
За оптимално покривање потреба за свим есенцијалним аминокиселинама, комбинујте разноврсне протеинске изворе — сурутку, јаја, махунарке и житарице. При интензивним тренинзима, допуна са BCAA (леуцин, изолеуцин, валин) може помоћи у опоравку мишића и смањити катаболизам.
🧭 Када изабрати шта?
- Изаберите самосталне аминокиселине, ако циљате брзу апсорпцију за одређену сврху (нпр. опоравак након тренинга) или имате специфични недостатак.
- Изаберите протеинске суплементе (који садрже различите аминокиселине), ако тражите свеобухватну подршку за раст мишића и општи опоравак.
- Дајте предност комплетним изворима протеина из хране, ако циљате дугорочно здравље, уравнотежену исхрану и унос свих есенцијалних хранљивих материја.
📖 Šta su Aminokiseline?
Aminokiseline su gradivni blokovi proteina. Povezuju se jedna s drugom kako bi formirale duge lance koji izgrađuju mišiće, enzime i druge važne telesne strukture. Postoji 20 osnovnih aminokiselina, od kojih su 9 esencijalne, što znači da ih telo ne može samo proizvesti.
⚖️ Prednosti i nedostaci
| ✅ Prednosti | ❌ Nedostaci |
|---|---|
|
|
🗣️ Objašnjeno jednostavno
Aminokiseline su osnovni gradivni elementi proteina, kao ciglice od kojih se grade tvoji mišići. Postoje različite vrste, neke tvoje telo samo pravi, druge moraš unositi hranom. Super su važne za mišiće, kožu, kosu i skoro sve u tvom telu.